Bienvenidos
La Dirección Regional de Medicamentos, Insumos y Drogas (DIREMID), como Autoridad Regional de Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios reconocida según Ley de Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios (Ley Nº 29459) es la responsable de garantizar y mejorar el acceso a Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios, de Calidad, especialmente a las poblaciones menos favorecidas de la región.

CONTÁCTANOS
diremid_ayacucho@saludayacucho.gob.pe
INFORMACIÓN INSTITUCIONAL
-
¿Qué Hacemos?
Planificar, organizar, evaluar, supervisar y controlar en lo que corresponda a la calidad, uso, comercialización y suministro de Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios en concordancia con las normas, lineamientos y políticas del sector salud.
-
Misión

-
Visión

-
Objetivo General
Garantizar el acceso a productos farmacéuticos, dispositivos médicos y productos sanitarios de calidad a la población de la Región de Ayacucho. -
Objetivos Especificos
<> Garantizar el acceso a productos farmacéuticos, dispositivos médicos y productos sanitarios, especialmente a las poblaciones vulnerables.
<> Fomentar y promover el uso racional de medicamentos, en atención en salud, en los profesionales de la salud y en la comunidad (Art. 30 de la Ley Nº 29459).
<> Velar por la salud pública a través de las acciones de fiscalización, control y vigilancia de la comercialización de productos farmacéuticos, dispositivos médicos y productos sanitarios en establecimientos públicos y privados de la región (Art. 44 de la Ley Nº 29459 y Art. 6 del DS-014-2011-SA).
ORGANIGRAMA
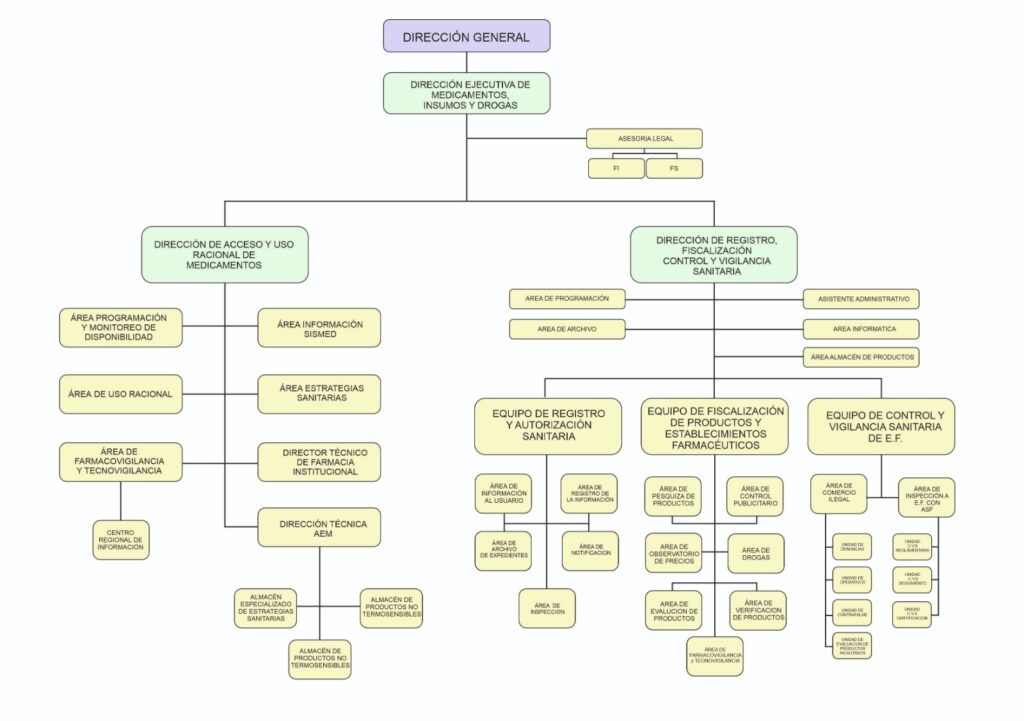
DIRECTORIO RESPONSABLES
Área/unidades

Direccion De Registro, Fiscalizacion, Control Y Vigilancia Sanitaria

Dirección Ejecutiva de Medicamentos, Insumos y Drogas

Direccion De Acceso y Uso Racional de Medicamentos

Direccion De Registro, Fiscalizacion, Control Y Vigilancia Sanitaria

Dirección Ejecutiva de Medicamentos, Insumos y Drogas

Direccion De Acceso y Uso Racional de Medicamentos

Direccion De Registro, Fiscalizacion, Control Y Vigilancia Sanitaria

Dirección Ejecutiva de Medicamentos, Insumos y Drogas

Direccion De Acceso y Uso Racional de Medicamentos
DOCUMENTOS
[table “” not found /]
NORMATIVA | RECURSO |
|---|---|
| DS 014-2011-MINSA_Reglamento de Establecimientos Farmaceuticos | |
| DS 026-2019-SA_Reglamento DU 007-2019 | |
| DU 007-2019_Medic Esenciales DCI OF | |
| RM 091-2023-MINSA_Modificar Art. RM 554-2022 | |
| RM 302-2020-MINSA_Listado Medic Esenciales DCI OF | |
| RM 481-2023-MINSA_Amplian Plazos RM 554-2022 | |
| RM 554-2022-MINSA_Manual BPOF |
- Ficha Informativa
- Alertas
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 04/04/2025
Comercialización Ilegal de Productos Farmacéuticos de Dudosa Procedencia a Través de Plataformas de Comercio Electrónico, que Ponen en Riesgo la Salud de la Población.
- 04/04/2025
Actualización de Sospechas de Reacciones Adversas Graves Con un Lote de Cloruro de Sodio.
- 26/03/2025
Sospechas de Reacciones Adversas Graves con un Lote de Cloruro de Sodio.
- 24/03/2025
Falsificación del Producto Inmunoglobulina Humana ANTI-D 300 mcg, (Rho) Solución Intectable, Notificado por el CECMED DE CUBA.
- 14/03/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitria.
- 14/03/2025
Retiro Voluntario del Dispositivo Médico de Diagnóstico IN VITRO VENTANA anti-CD10(SP67) Rabbit Monoclonal Primary Antibody
- 14/03/2025
Actualización sobre la Falsificación y Comercialización Irregular del Producto PROLIA (Denosumab) 60 mg/ml, Notificado por la COFEPRIS de Mexico.
- 11/03/2025
Producto Farmacéutico Falsificado Incautado en Acciones de Control y Vigilancia Sanitaria.
- 11/03/2025
Falsificación del Producto PENTREXYL (Ampicilina) 500 MG Cápsulas, Notificado por la COFEPRIS de Mexico.
- 11/03/2025
Falsificación del Producto NOVOSEVEN RT (Eptacog alfa (activado) 2 MG (100 KUI) Solución Inyectable, Notificado por la COFEPRIS de Mexico.
- 11/03/2025
Falsificación del Producto EDEGRA (Sildenafilo) 100 MG Tabletas, Notificado por la COFEPRIS de Mexico.
- 11/03/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria
- 11/03/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria
- 11/03/2025
Retiro del Mercado de un Lote de Producto Observado por Resultado Critico de Control de Calidad.
- 11/03/2025
Retiro del Mercado de un Lote de Dispositivo Medico Observado por Resultado Crítico de Control de Calidad.
- 11/03/2025
Retiro del Mercado de un Lote de Dispositivo Medico Observado por Resultado Crítico de Control de Calidad.
- 04/03/2025
Retiro del Mercado de un Lote de Farmacéutico Observado por Resultado Crítico de Control de Calidad.
- 04/03/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia.
- 04/03/2025
Retiro del Mercado de un Lote de Dispositivo Medico Observado por Resultado Crítico de Control de Calidad.
- 26/02/2025
ÁCIDO VALPROICO: Posible Riesgo de Trastornos del Desarrollo Neurológico en Niños por Exposición del Padre.
- 26/02/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 19/02/2025
Producto Sanitario Falsificado Incautado en Acciones de Control y Vigilancia Sanitaria.
- 19/02/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 19/02/2025
Ceftriaxona y soluciones con Calcio: Actualización de Información de Seguridad.
- 19/02/2025
Inhibidores de SGLT-2(CANAGLIFLOZINA, DAPAGLIFLOZINA Y EMPAGLIFLOZINA): Riesgo de Cetoacidosis Diabética Prolongada.
- 19/02/2025
TOFACITINIB: Riesgo de Leucoencefalopatía Multifocal Progresiva (LMP)
- 07/02/2025
Productos Sanitarios Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 07/01/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 07/02/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria
- 07/02/2025
Suspensión de Comercialización de Productos Farmacéuticos que Contienen Ranitidina.
- 07/02/2025
Dispositivo Médicos Falsificado Incautado en Acciones de Control y Vigilancia Sanitaria
- 28/01/2025
Retiro del Mercado de un Lote de Dispositivo Medico Observado por Resultado Crítico de Control de Calidad.
- 28/01/2025
Retiro de Mercado de un Lote de Producto Farmacéutico Observado por Resultado Crítico de Control de Calidad.
- 28/01/2025
Riesgo de Presencia de Impurezas de Nitrosaminas en Medicamentos Conteniendo Ranitidina.
- 14/01/2025
Inhibidores de Puntos de Control Inmunologico (IPILIMUMAB NIVOLUMAB y PEMBROLIZUMAB): Riesgos de Síndrome de Liberación de Citocinas.
- 14/01/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 14/01/2025
Productos Farmacéuticos Falsificados Incautados en Acciones de Control y Vigilancia Sanitaria.
- 14/01/2025
Productos Cosméticos Comercializados a través del Comercio Electrónico Podrían Ocasionar un Riesgo para la Salud Pública.
- 14/01/2025
Seguridad para Productos Farmacéuticos que Contienen ÁCIDO VALPROICO
- 06/02/2025
Seguridad para Productos Farmacéuticos que Contienen INHIBIDORES DE SGLT-2.
- 24/01/2025
Seguridad para Productos Farmacéuticos que Contienen TOFACITINIB.
- 24/01/2025
Seguridad para Productos Farmacéuticos que Contienen CABERGOLINA
- 28/01/2025
Seguridad para Productos Farmacéuticos que Contienen CEFTRIAXONA..
- 03/02/2025
CAMPAÑAS Y EVENTOS
CAMPAÑA INFORMATIVA POR EL DÍA DEL QUÍMICO FARMACEÚTICO





















REUNIÓN MANUAL BPOF



























